1 million d’utilisateurs ! Histoire de l’implant Cochléaire

L’implant cochléaire est la prothèse neuronale la plus réussie, avec un million d’utilisateurs dans le monde. Les chercheurs ont conçu des implants multicanaux modernes, permettant aux personnes implantées d’atteindre une reconnaissance correcte des phrases dans le calme de 70 à 80 %, en moyenne. Les chercheurs ont également utilisé l’implant cochléaire pour aider à comprendre les mécanismes de base qui sous-tendent le volume sonore (l’intensité), le ton et la plasticité cérébrale. Alors que les progrès du traitement initial ont amélioré la reconnaissance de la parole dans le bruit, la reconnaissance de la parole dans le calme par l’implant unilatéral a atteint un plateau depuis le début des années 1990. Ce manque de progrès appelle à prendre des mesures pour repenser l’interface de stimulation cochléaire et à collaborer avec la communauté neurotechnologique en général.
Introduction
Les implants cochléaires sont la prothèse neuronale la plus réussie, ayant restauré l’audition fonctionnelle à un million de personnes partiellement ou totalement sourdes dans le monde. L’implant cochléaire permet non seulement à un utilisateur adulte moyen d’avoir une conversation téléphonique sans lire sur les lèvres, mais, plus important encore, il fournit un mode permettant à un enfant de développer un langage normal. En comparaison, moins d’un millier de personnes non voyantes ont reçu un implant rétinien pour restaurer leur vision et 208 000 personnes ont bénéficié d’une stimulation cérébrale profonde pour traiter des troubles neurologiques et neuropsychiatriques en 2021.
Le marché des implants cochléaires est dominé par Cochlear Limited (Sydney, Australie), qui a vendu 650 000 implants au cours des 40 dernières années (Cochlear Limited, 2021). En tant que société privée, Med El (Innsbruck, Autriche) n’a pas divulgué le nombre d’implants vendus, mais a indiqué en 2015 qu’elle avait dépassé Cochlear en tant que premier acteur en Europe et qu’elle était clairement le deuxième plus grand fabricant (Zeng et al., 2015). Advanced Bionics (Valencia, CA) n’a pas non plus dévoilé son nombre d’implants vendus, mais sa société mère, Sonova (Stäfa, Suisse), a déclaré un chiffre d’affaires total de 180 M USD pour le segment des implants cochléaires en 2021, soit environ un cinquième du chiffre d’affaires de Cochlear (Sonova, 2021). En 2021, Nurotron (Hangzhou, Chine) a vendu plus de 20 000 dispositifs, tandis qu’Oticon Medical, anciennement Neurelec (Vallauris, France), en a vendu 16 500. D’autres sociétés plus petites ont vendu plusieurs milliers de dispositifs (par exemple, Listent, Shanghai, Chine) où sont implanté plusieurs centaines de dispositifs dans le cadre de leurs essais cliniques (par exemple, AIC Aiyisheng, Shenyang, Chine ; Shree Coratomic Limited, Madhya Pradesh, Inde ; Todoc, Séoul, Corée). Il y a également une diminution du nombre d’utilisateurs actifs de plusieurs milliers de 3M/House (House et Urban, 1973) et Inraid (Eddington, 1978), qui ont été développés dans les années 1970 mais qui ont été progressivement retirés du marché dans les années 1990. La figure 1 montre la part cumulée du marché d’un million d’implants cochléaires.
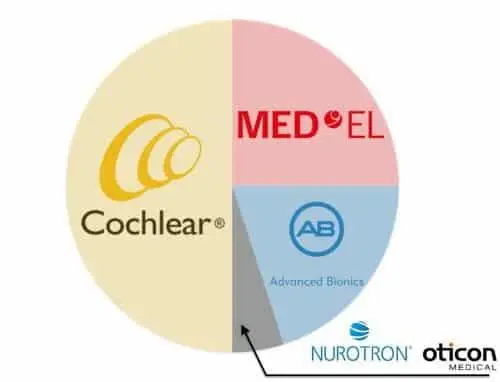
Pour célébrer le millionième implant cochléaire, cet article, rédigé par Fan-Gang Zeng, décrit d’abord les étapes importantes de la recherche et du développement qui sont à l’origine de ce dispositif médical remarquable. Ensuite, il examine la science à l’origine de la prothèse neuronale la plus réussie et évoque du goulot d’étranglement actuel qui limite ses performances. Enfin, l’article évoquera les voies permettant d’améliorer les performances des implants cochléaires et mettra en évidence les opportunités de collaboration entre le domaine des implants cochléaires et la communauté des technologies neuronales en général.
Les étapes de la recherche et du développement des implants cochléaires
Trois étapes sont nécessaires à la réussite d’un dispositif médical : la faisabilité, la sécurité et l’efficacité. La faisabilité des implants cochléaires remonte à Volta qui, en 1800, a démontré qu’une stimulation électrique pouvait provoquer l’audition. La figure 2 montre les trois étapes qui ont permis d’établir la sécurité et l’efficacité des implants cochléaires modernes. William House, père de la neurotologie, a mis au point le premier implant cochléaire approuvé par la FDA, doté d’une liaison de transmission passive à bobine et d’une électrode intra-cochléaire unique. Le dispositif monocanal House était essentiel à la sécurité et à l’acceptation de l’implant cochléaire, mais il ne pouvait produire qu’un niveau minimal de reconnaissance de phrases ouvertes, sa fonction étant principalement de faciliter la lecture labiale et d’améliorer la perception des sons de l’environnement (House et Berliner, 1986). Graeme Clark a dirigé le développement d’un implant cochléaire multicanal pour le dispositif Nucleus-22, qu’il a décrit comme « une deuxième percée », car il permettait aux « adultes sourds post-linguaux non seulement de percevoir le bruit complexe de leur environnement acoustique, mais aussi de reconnaître des mots avec et même sans repères visuels » (Clark et al., 1987). Wilson et al. (1991) ont mis au point la stratégie « Continuous-Interleaved-Sampling » ou CIS, qui est devenue, depuis, la norme industrielle de facto permettant à l’utilisateur moyen d’atteindre un niveau élevé (70%-80% d’exactitude) de reconnaissance de phrases dans le calme sans lecture labiale.

Les sciences de l’audition et de la parole à l’origine de l’implant cochléaire
Les implants cochléaires multicanaux modernes ont été conçus en tenant compte des connaissances approfondies de la recherche sur l’audition et la parole. Du côté de l’audition, la conception a suivi les principes de codage du ton des sons, tant au niveau du lieu que du moment. La disposition des électrodes respecte la structure tonotopique de l’oreille interne (Greenwood, 1961), tandis que le nombre d’électrodes correspond approximativement aux 24 filtres auditifs ou bandes critiques (Zwicker, 1961). Les impulsions électriques peuvent être soit périodiques, soit aléatoires, selon les attributs du signal vocal, car elles produisent des schémas de décharge nerveuse qui sont en phase asservie avec la forme d’onde du stimulus (Kiang et Moxon, 1972). En ce qui concerne la parole, le traitement du signal de l’implant cochléaire reposait sur les théories acoustiques de la production et de la perception de la parole.
Source et filtre pour représenter la structure spectrale fine et l’enveloppe
Fant (1970) a séparé la parole en deux parties : (1) une source qui est soit un signal périodique provenant de la vibration des cordes vocales, soit un signal bruyant provenant du flux d’air expulsé par le poumon et (2) un filtre qui représente les fréquences de résonance du conduit vocal. La figure 3 montre le spectre d’une source périodique, qui se compose d’harmoniques, la première harmonique étant appelée fréquence fondamentale ou F0 ; cette source est façonnée spectralement par la résonance des voies vocales ou fréquences des formants, les deux premiers formants étant étiquetés F1 et F2. La source contribue à l’identité et à la qualité du locuteur, tandis que le filtre contribue à l’intelligibilité de la parole. Par exemple, on peut doubler la F0 pour qu’un locuteur masculin sonne comme un locuteur féminin (deuxième rangée), ou remplacer la source périodique par une source de bruit pour obtenir un discours chuchoté (troisième rangée). Aucune de ces modifications de la source n’altère l’intelligibilité de la parole (dans le calme) tant que le filtre du conduit vocal (c’est-à-dire les formants) reste intact.
Les premiers implants cochléaires multi-électrodes, en particulier le dispositif Nucleus qui a connu le plus grand succès, ont été conçus sur la base de ce modèle de source et de filtre. Le premier processeur vocal portable Nucleus encodait la source soit avec un taux de stimulation à F0 pour un son voisé, soit un taux aléatoire pour un son aphone, mais il n’extrayait que le second formant ou F2 du son pour encoder ses informations de filtre (Tong et al., 1980). Comme le F0 ne contribue pas à l’intelligibilité et que le F2 n’est pas adéquat pour encoder l’information consonantique (Blamey et al., 1987), ce premier processeur vocal produisait une reconnaissance de phrase correcte à 10%-20%. Même lorsque le F1 a été ajouté plus tard, la reconnaissance des phrases ne s’est améliorée que de 30 à 40 % (Dowell et al., 1986). Le niveau relativement faible de reconnaissance des phrases était dû à une difficulté technique de l’époque et à une limitation fondamentale des implants cochléaires. La difficulté résidait dans le fait que les puces de traitement numérique du signal de l’époque ne pouvaient traiter que des algorithmes moins sophistiqués (c’est-à-dire la détection du passage par zéro), ce qui donnait une estimation grossière de la fréquence instantanée du signal et était sensible au bruit de fond. Même si ces fréquences fondamentales et de formants pouvaient être mesurées avec précision, ce qui est trivial avec la technologie actuelle, elles ne peuvent pas être cartographiées avec le(s) bon(s) emplacement(s) cochléaire(s) par les implants cochléaires. Non seulement l’emplacement des électrodes intra-cochléaires varie grandement en raison de la profondeur d’insertion, de la flexion ou même d’un placement incorrect (par exemple, scala vestibuli), mais les individus ont également différents degrés et modèles de survie des nerfs. Cette variabilité individuelle est encore compliquée par la grande dispersion de la stimulation électrique, ce qui rend impossible la reproduction de l’organisation tonotopique normale très précise qui est essentielle à l’encodage de la fréquence spécifique au lieu (Zeng et al., 2014). Une approche différente était nécessaire pour améliorer les performances de reconnaissance vocale des implants cochléaires.

Vocodeurs pour représenter l’enveloppe temporelle
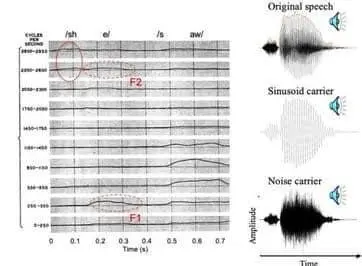
Dudley (1939) a montré dans sa célèbre invention de « vocodeur » à dix canaux que, pour rendre la parole intelligible, il n’est pas nécessaire d’obtenir avec précision les fréquences des formants, qui sont grossièrement représentées par la haute énergie de la modulation d’amplitude lente (∼10 Hz) extraite de chaque canal. Cette modulation lente de l’amplitude a été appelée indice de l’enveloppe temporelle (Van Tasell et al., 1987 ; Rosen, 1992), qui s’est avérée être la clé de la réalisation des performances de haut niveau (70-80% de reconnaissance correcte des phrases dans le calme) des implants cochléaires modernes. Plusieurs études ont contribué à ce succès. Premièrement, les indices de l’enveloppe temporelle provenant de trois canaux seulement sont suffisants pour la reconnaissance vocale (Shannon et al., 1995). Deuxièmement, les porteurs, qu’il s’agisse de sinusoïdes ou de bruits à bande étroite, ne sont pas importants (Dorman et al., 1997). Le panneau supérieur droit de la figure 4 montre la forme d’onde originale pour une syllabe /sa/ et son enveloppe (ligne rouge sur le côté positif de la forme d’onde), tandis que les panneaux inférieurs montrent la sinusoïde et la porteuse de bruit, modulées respectivement par l’enveloppe /sa/. Troisièmement, en raison du degré élevé de verrouillage de phase de la décharge du nerf auditif à la stimulation électrique (Dynes et Delgutte, 1992), les utilisateurs d’implants cochléaires peuvent tirer pleinement parti des indices de l’enveloppe temporelle, étant capables de détecter des fluctuations encore plus faibles que celles des auditeurs acoustiques normaux (Shannon, 1992). Enfin, Wilson et al. (1991) ont réuni tous ces éléments dans la stratégie CIS, dans laquelle l’enveloppe temporelle a été correctement extraite et comprimée pour correspondre à la gamme dynamique de l’utilisateur de l’implant, puis utilisée pour moduler en amplitude une porteuse d’impulsion biphasique à débit relativement élevé (∼1000 Hz), qui a été entrelacée entre les électrodes pour éviter les interactions associées à la stimulation simultanée. Le CIS et d’autres implémentations similaires de cette époque [par exemple, n-of-m (McDermott et al., 1992)] sont restés la pierre angulaire de tous les implants cochléaires modernes.
Les implants cochléaires comme outil de recherche
Les implants cochléaires ont également été utilisés comme outil de recherche pour approfondir notre compréhension des processus de l’audition et de la parole, voire pour découvrir de nouveaux mécanismes. Le codage de l’intensité sonore en est un exemple. Il est bien connu que la sonie croît comme une fonction de puissance de l’intensité sonore. La théorie classique veut que cette fonction puissance soit due à la non-linéarité de la cochlée (Stevens, 1961), le cerveau se comportant comme un dispositif linéaire (Krueger, 1989). La cochlée étant contournée dans l’audition électrique, on pourrait prédire une fonction d’intensité sonore linéaire chez les utilisateurs d’implants cochléaires, si la théorie classique était vraie. Au lieu de cela, on a trouvé une fonction d’intensité sonore exponentielle, suggérant un mécanisme non linéaire en deux étapes, de compression à expansion, dans le codage de l’intensité sonore (Zeng et Shannon, 1994). Ce modèle actif de sonie a été intégré pour produire une théorie unifiée de la perception de l’intensité auditive (Zeng, 2020) et expliquer les acouphènes, ce qui serait difficile pour un cerveau passif et linéaire (Zeng, 2013). Un autre exemple est le codage de la hauteur, qui a traditionnellement adopté une théorie duplex. Pour les tons de haute fréquence, la hauteur s’appuie sur un code de lieu, correspondant à l’organisation tonotopique susmentionnée (Zwislocki, 1991).
Pour les sons basse fréquence, la tonalité s’appuie sur un code temporel, dans lequel la fréquence du son est l’inverse de l’intervalle de décharge nerveuse (Rose, 1967). On pensait que ces deux codes étaient indépendants l’un de l’autre, leurs contributions relatives étant depuis longtemps un sujet de débat dans le domaine de l’audition (Burns et Viemeister, 1976 ; Cariani et Delgutte, 1996 ; Oxenham et al., 2004).
Dans les implants cochléaires, l’emplacement et le moment de la stimulation peuvent être manipulés indépendamment afin de tester la théorie classique du duplex. En effet, la hauteur électrique dépend à la fois de l’emplacement et du moment de la stimulation, ce qui suggère que « les modèles modernes de hauteur des sons complexes devraient prendre en compte les informations de lieu absolu » (Zeng, 2002). Oxenham et al. (2004) ont utilisé des « stimuli transposés » dans l’audition acoustique pour arriver à la même conclusion.
Enfin, les implants cochléaires ont été utilisés pour illustrer l’importance de la plasticité cérébrale. Le cerveau est un dispositif dynamique qui s’adapte aux changements. Non seulement la gamme dynamique électrique s’étend (Henkin et al., 2006), mais la hauteur du son électrique change également avec l’expérience des implants cochléaires au fil du temps (Reiss et al., 2007).
La stimulation électrique a été utilisée pour étudier la plasticité cérébrale à la suite d’une perte auditive et de la restauration de l’audition par un implant cochléaire (Ryugo et al., 2005). La comparaison des potentiels évoqués entre les personnes implantées et les personnes entendantes a révélé une période critique pour la maturation du cerveau et peut-être le développement du langage (Ponton et Eggermont, 2001 ; Sharma et al., 2002 ; Harrison et al., 2005).
La recherche sur les implants cochléaires chez les animaux et les humains a révélé une réorganisation corticale non seulement dans la zone auditive, mais aussi dans les régions visuelles et somatosensorielles du cerveau (Lee et al., 2001 ; Land et al., 2016). Bien qu’il ne soit pas clair si ces changements dans le cerveau sont bons ou mauvais, le suivi de la plasticité peut conduire à des améliorations dans la capacité à prédire et à expliquer les résultats des implants cochléaires (Feng et al., 2018).
Solutions au goulot d’étranglement des performances de l’implant cochléaire
Malgré les découvertes importantes et les progrès technologiques, de l’amélioration du traitement initial (Boyle et al., 2009) à l’audition électrique bilatérale et à la stimulation électro-acoustique, les performances de base d’un utilisateur d’implant unilatéral moyen sont restées inchangées au cours des 30 dernières années (Zeng, 2017).
Comparés aux auditeurs normo-entendants, les utilisateurs actuels d’implants cochléaires éprouvent toujours d’énormes difficultés à identifier la parole dans le bruit de fond, à localiser les sons et à distinguer la mélodie et le timbre, sans parler de l’appréciation de la subtilité et de la richesse d’une musique plus complexe comme une symphonie (McDermott, 2004 ; Kerber et Seeber, 2012 ; Limb et Roy, 2014 ; Fowler et al., 2021). Ce goulot d’étranglement de 30 ans n’est pas dû à un manque d’efforts, car de nombreuses idées innovantes ont été essayées mais n’ont pas encore produit d’améliorations significatives des performances.
Ces idées comprenaient, par exemple, l’augmentation du taux de stimulation pour simuler l’activité spontanée du nerf auditif (Rubinstein et al., 1999), l’encodage par modulation de fréquence pour restaurer la structure fine (Nie et al., 2005), l’échantillonnage entrelacé asynchrone pour encoder simultanément l’enveloppe et la phase (Sit et al., 2007), la génération de schémas de décharge normaux du nerf auditif via un modèle de calcul (Chen et al., 2005 ; Erfanian Saeedi et al., 2017), la réduction de la propagation de l’excitation via une stimulation bipolaire et tripolaire ou une forme d’onde asymétrique (Berenstein et al., 2008 ; Zhu et al., 2012 ; Carlyon et al., 2014), et la création de canaux virtuels via une stimulation à électrodes multiples (Donaldson et al., 2011).
Pour remédier à ce goulot d’étranglement, les implants cochléaires actuels doivent améliorer à la fois le codage et la transmission des indices spectraux et temporels de structure fine (Zeng et al., 2005). Jusqu’à présent, la plupart des idées se sont concentrées sur le codage de ces indices de structure fine dans le processeur vocal, avec peu ou pas d’investissement dans l’interface critique électrode-neurone.
En fait, la conception fondamentale des 12-24 électrodes de la scala tympani est restée inchangée depuis sa création, à l’exception des améliorations et des modifications cosmétiques de la forme, de la taille et de la position des électrodes ou de la longueur, de l’épaisseur et de la courbure du réseau. L’utilisation continue de cette même conception d’électrode constitue le goulot d’étranglement qui limite les performances de l’implant cochléaire. Tant que l’interface électrode-neurone n’aura pas été repensée pour pouvoir transmettre les signaux nécessaires, le traitement du signal dans le processeur vocal ne permettra pas d’améliorer les performances. Plusieurs idées novatrices ont été proposées pour modifier l’interface électrode-neurone afin d’améliorer les performances des futurs implants cochléaires. L’une d’entre elles consiste à implanter directement un réseau d’électrodes pénétrantes dans le nerf auditif, ce qui, dans un modèle animal, a permis de réduire à la fois le seuil de stimulation et la propagation de l’excitation par rapport aux implants cochléaires classiques (Middlebrooks et Snyder, 2007). Deux études financées par le NIH testent la faisabilité de cet implant nerveux pénétrant chez l’homme (5R01-DC017182 par John Middlebrooks et Harrison Lin à l’Université de Californie Irvine et 5UG3-NS107688 par Hubert Lim à l’Université du Minnesota). L’autre idée adopte une approche opposée, selon laquelle, au lieu d’implanter les électrodes dans le nerf auditif, des facteurs neurotrophiques sont appliqués pour inciter le nerf auditif à se développer dans les électrodes cochléaires (Pinyon et al., 2014).
Cette approche combinant l’implant cochléaire et l’administration de médicaments permet non seulement d’améliorer les performances de l’implant cochléaire, mais aussi d’administrer des médicaments dans l’oreille interne. Une troisième idée, plus agressive que les deux précédentes, utilise la stimulation lumineuse pour restaurer les schémas normaux d’excitation dans la cochlée. La recherche sur les animaux a démontré la faisabilité et l’innocuité de cette technique, et des tentatives pour réduire la puissance et la taille du système de stimulation lumineuse adapté à l’usage humain (Keppeler et al., 2020 ; Littlefield et Richter, 2021).
Conclusion
Le domaine de l’implant cochléaire a été et est toujours un leader en matière de technologie neuronale, mais d’autres domaines sont en train de rattraper leur retard et pourraient probablement prendre le relais dans un avenir proche. Par exemple, la stimulation de la moelle épinière est désormais utilisée pour gérer la douleur chez environ 50 000 patients par an (Sdrulla et al., 2018), ce qui approche le nombre annuel d’implantations cochléaires (∼65 000).
Le développement technologique des implants cochléaires, ou récemment leur absence, a pris du retard par rapport à celui des interfaces cerveau-ordinateur, qui emploient des milliers d’électrodes ayant à la fois une capacité d’enregistrement et de stimulation, une communication sans fil protégée et continue, et une autonomie prolongée de la batterie sans recharge jusqu’à 20 ans dans le corps (De Wachter et al., 2020 ; Luan et al., 2020).
Par conséquent, un implant cochléaire totalement implantable reste insaisissable, bien que cette idée ait été proposée depuis des décennies et qu’elle aurait probablement un impact considérable sur la commodité, la stigmatisation et le mode de vie. Bien que les chercheurs spécialisés dans les implants cochléaires aient innové en déplaçant le site de stimulation de la cochlée vers le tronc cérébral auditif et le mésencéphale (Brackmann et al., 1993 ; Lim et al., 2008), aucune avancée récente n’a été enregistrée dans cette méthodologie.
En revanche, les chercheurs dans le domaine de la vision poursuivent activement la mise en place d’un implant cortical à haute densité dans l’espoir de restaurer non seulement l’acuité visuelle mais aussi la vision des couleurs (Chen et al., 2020 ; Fernandez et al., 2021 ; Towle et al., 2021). Poussés par l’actuelle NIH Brain Initiative et des efforts similaires à l’échelle mondiale, les neuroscientifiques et les neuroingénieurs se précipitent vers les premières applications humaines qui espèrent traiter ou prévenir un large éventail de maladies neurologiques et psychiatriques. Tout en célébrant cette remarquable réalisation du millionième implant cochléaire, nous pouvons et devons appliquer notre expérience et notre expertise pour aider les « nouveaux venus » à éviter les pièges de l’innovation tout en leur empruntant de nouvelles idées pour restaurer, voire améliorer, l’audition normale.




